据我们所知,人类基因估计约有25000个基因,而蛋白质的总数预计要多得多,估计超过100万个。单个基因可以编码多种蛋白质。除了替代剪接mRNA编辑作为蛋白质复杂性的来源,蛋白质的翻译后修饰(PTMs)可以进一步促进从基因组水平到蛋白质组水平的复杂性。
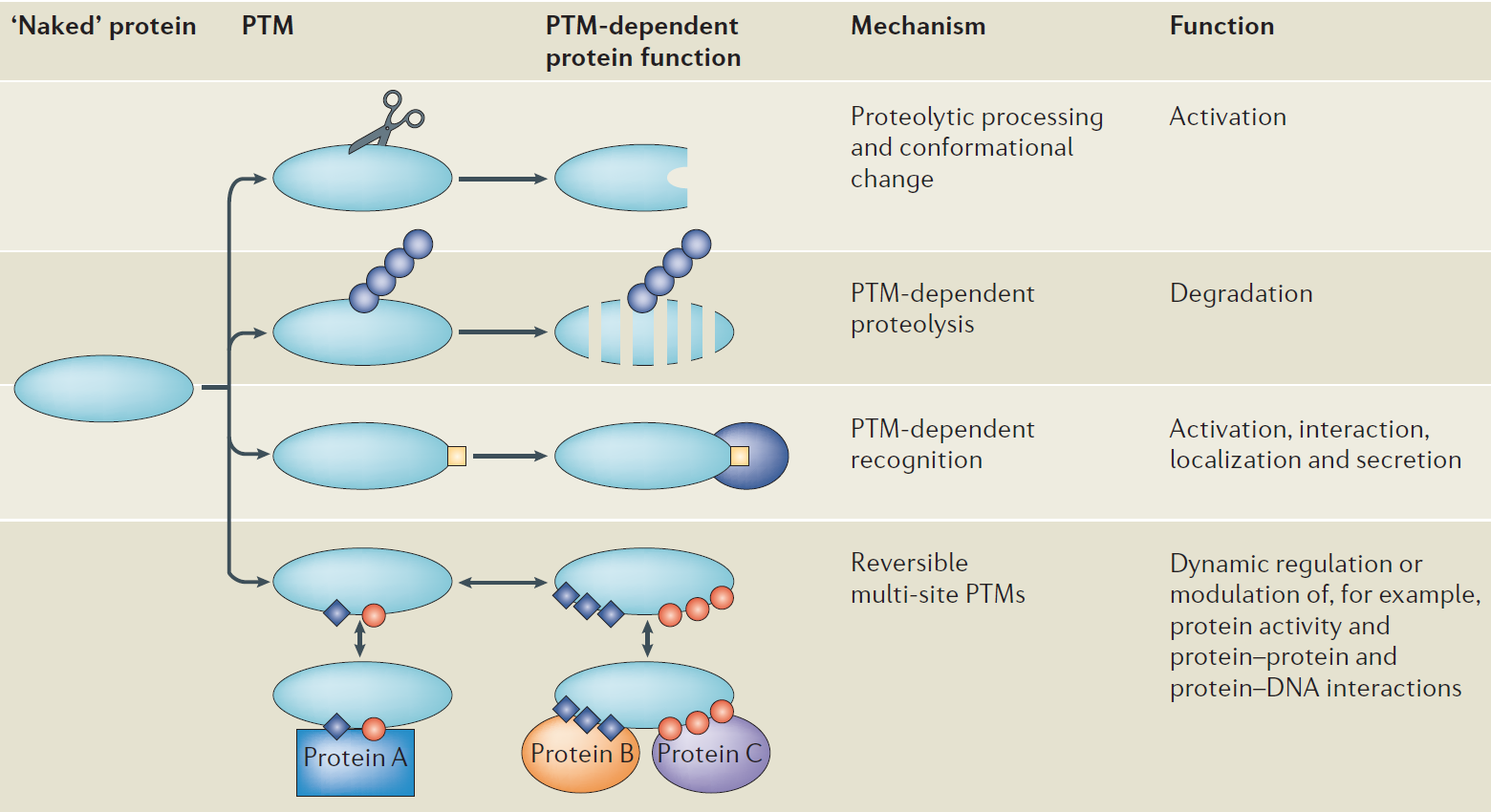
PTMs是对蛋白质结构的化学改变,通常是由极其特异的底物酶催化的,而这些酶本身受到PTMs的严格控制。由于许多类型的PTMs共价附着在蛋白质的氨基酸残基上,因此基因产物具有丰富的多样性。PTMs有不同的作用。蛋白水解过程和构象变化通过裂解蛋白质中的不同位点而导致激活。此外,PTMs可以标记破坏蛋白,如聚泛素化介导的蛋白降解。此外,经ptm依赖的识别可导致激活、相互作用、定位和分泌。PTMs可能诱导构象变化或形成对接位点,介导分子识别,稳定蛋白-配体和蛋白-蛋白相互作用。通过可逆的多位点PTMs,它们可以快速、动态地调节或调节蛋白质活性、蛋白质-蛋白质和蛋白质- dna相互作用。
图1所示。翻译后修饰的作用机制(Jensen O N, 2006)
经鉴定的创伤后应激障碍有200多种。它们可以影响细胞功能的许多方面,如代谢、信号转导和蛋白质稳定性。接下来,我们将简要介绍一些常见的PTMs,包括磷酸化、糖基化、甲基化、乙酰化和泛素化。
磷酸化
蛋白质磷酸化,其中通过添加共价结合的磷酸酯基团通过蛋白激酶磷酸化氨基酸残基,是在信号转导中使用的最广泛的PTM。通过激酶完成磷酸化,并通过发挥相反的磷酸酶进行去磷酸化。在真核细胞中,约86.4%的蛋白质磷酸化事件发生在丝氨酸(Ser或S)上,而11.8%蛋白磷酸化事件发生在苏氨酸上,而酪氨酸残基仅为1.8%。蛋白质磷酸化在许多过程中起着极其重要的作用,包括中介代谢,转录,细胞周期进展,分化等。
糖基化
糖基化,即糖基与蛋白质的结合,对细胞中许多生物过程都是至关重要的。糖基化有不同的类型。n -连接糖基化包括糖分子与氮原子的连接,氮原子是蛋白质的天冬酰胺(Asn)残基的酰胺氮。o型糖基化是指在蛋白质的氨基酸残基中,糖分子与氧原子的结合。c -甘露糖基化是通过C-C键将α-甘露糖基残基连接到Trp的C-2上。磷酸糖基化是指糖通过磷酸二酯键附着在蛋白质上。糖基化是糖基化的一种特殊形式,在糖基化过程中,蛋白质附着在脂质锚上。
甲基化
蛋白质甲基化涉及将甲基添加到蛋白质氨基酸中。精氨酸甲基可以作为转录的表观遗传调节器和预mRNA剪接,DNA损伤信号,mRNA翻译和细胞信号传导中发挥重要作用。据报道,甲基化可以发生在20个常见氨基酸残基的至少九个侧链上,包括精氨酸,赖氨酸,组氨酸,蛋氨酸,半胱氨酸,谷氨酰胺,天冬酰胺,谷氨酸和天冬氨酸。其中,精氨酸和赖氨酸是迄今为止最常见的甲基化残基。此外,精氨酸或赖氨酸的甲基化不会影响这些残留物的总电荷,即使甲基化时,它们的侧链也保持正电荷。赖氨酸残留物可以甲基化至多三次,高达两次的精氨酸残留物。甲基是最小的PTMS之一,并且对改性侧链的“空间体积”相对较少。
乙酰化作用
蛋白质乙酰化是乙酰辅酶A (Ac-CoA)产生的乙酰基转移到多肽链上特定位点的过程。蛋白质的乙酰化可以通过酶促和非酶促过程进行。在人类中,80-90%的蛋白质在其新生多肽链的n端发生共翻译乙酰化。乙酰基可以在n端乙酰转移酶(NATs)的催化下从Ac-CoA转移到多肽的n端氨基上。赖氨酸残基ε-氨基可逆乙酰化是另一种常见类型,由赖氨酸乙酰转移酶(KATs)和赖氨酸脱乙酰酶(kdac)催化。此外,乙酰化干扰了代谢过程和能量稳态,这是由于特定kdac在乙酰化过程中消耗Ac-CoA,在去乙酰化过程中消耗NAD+。
泛素化
泛素涉及通过一组三种酶将多肽泛素与靶向蛋白质的附着,包括泛素活化酶E2,泛素 - 缀合酶E2和遍突粘蛋白连接酶E3。E1酶首先使用能量将ATP分子转化为AMP和焦磷酸(PPI)的能量来激活遍在蛋白分子的羧基末端。活化的泛素连接到E1活性位点半胱氨酸残基的硫。然后从E1至E2转移泛素,E3促进从E2转移到底物蛋白中。泛素可以通过蛋白酶体标记蛋白质以改变它们的细胞位置,影响它们的活性,并促进或预防蛋白质相互作用。
蛋白质PTM分析,包括改性类型和改性位点,对细胞生物学以及疾病诊断和预防尤为重要。
参考:
- 利用蛋白质组学解释蛋白质语言。分子细胞生物学杂志,2006,7(6):391。
- 螺旋R G.蛋白质糖基化:糖肽键的性质,分布,酶形成和疾病影响。糖血管学,2002,12(4):43R-56R。
- 陈志强,史玉华。蛋白质甲基化研究的曲折路径:里程碑和新前沿。分子细胞生物学,2017,18(8):517。
- 王Y C,Peterson S E,Loring J F.蛋白质翻译后的翻译修改和调节人干细胞中多能性。细胞研究,2014,24(2):143。
- Drazic A,MyklebustL M.等。蛋白质乙酰化的世界。生物化学与生物物理学报,2016,1864(10):1372-1401。